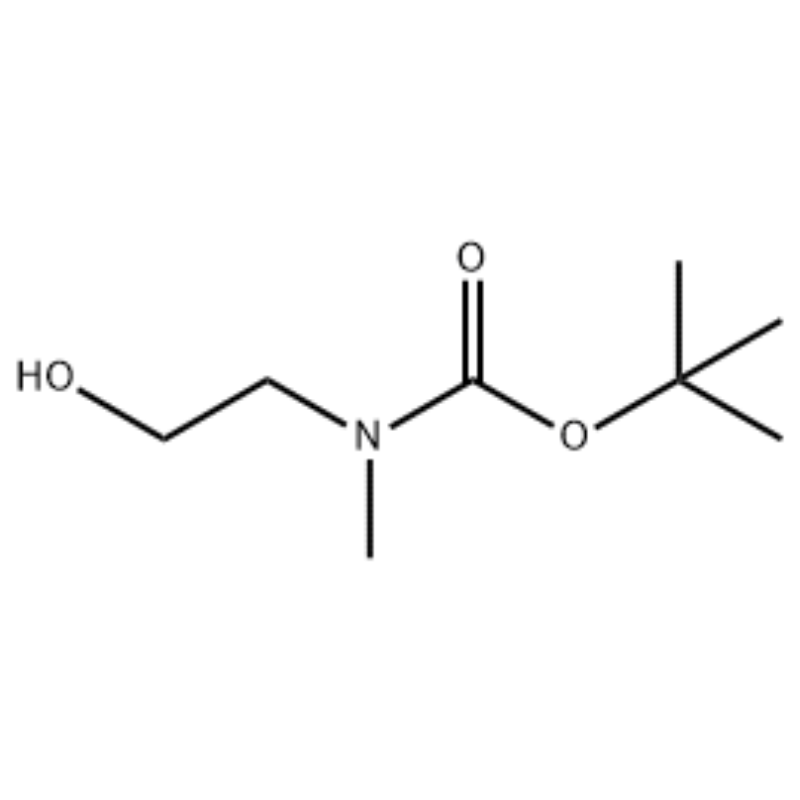
לתמיסה של 2-(מתילאמינו)אתנול (500 מ"ג, 0.53 מ"ל, 6.66 מ"ל) ב-CH2Cl2 (20 מ"ל) נוספה Boc2O (1.48 גרם, 6.79 ממול), ולאחר מכן ערבוב בטמפרטורת החדר למשך שעה.תמיסת התגובה חולצה עם מי מלח ו-CH2Cl2.השכבה האורגנית שהתקבלה כך יובשה על MgSO4 וסוננה.לאחר מכן, התסנין רוכז בוואקום לקבלת תרכובת האובייקט (שמן חסר צבע, כמותי);1H NMR (200 MHz, CDCl3) דלתא 3.74 (q, J= 10.5, 5.2 Hz, 2H) 3.25 (t, J= 5.2 Hz, 2H) 2.91 (s, 3H) 1.45 (s, 9H);ספקטרום מסה m/e (עוצמה יחסית) 144 (20) 102 (24) 57 (70) 44 (100).
דוגמה 38;N1-(3-פלואור-4-(2-(1-(2-(מתילאמינו)אתיל)-1H-אימידאזול-4-איל)תיאנו[3,2-ב]פירידין-7-אילוקסי)פניל)-N3 -(2-מתוקסיפניל)מלונמיד (96);שלב 1: tert-Butyl 2-hydroxyethyl(methyl)carbamate (97) (J. Med. Chem., 1999, 42, 11, 2008) לתמיסה של 2-(מתילאמינו)אתנול (5.0 גרם, 67 mmol) ב THF (50 מ"ל) ב-RT נוספה Boc2O (15.7 גרם, 72 mmol) ותערובת התגובה הועברה ב-RT למשך 4 שעות.תערובת התגובה רוכזה ליובש והתרכובת הכותרת 97 שימשה ישירות בשלב הבא ללא טיהור נוסף (11.74 גרם, 100% תשואה).MS (מ/ז): 176.2 (M+H).
הכנת l-2-[4-Bromo-2-(4-oxo-2-ftiotaioxo1hiazolidin-5-ylidenemefliyl)phenoxy]efliyl-3-efliyl-l-methylurea(Compoiotamd 161) שלב 1: סינתזה של t-butyl2- הידרוקסיאתיל מתיל קרבמט;לתמיסה של 2-(מתילאמינו)אתנול (500 מ"ג, 0.53 מ"ל, 6.66 מ"ל) ב-CH2Cl2 (20 מ"ל) נוספה BoC2O (1.48 גרם, 6.79 ממול), ולאחר מכן ערבוב בטמפרטורת החדר למשך שעה.תמיסת התגובה חולצה עם מי מלח ו-CH2Cl2.השכבה האורגנית שהתקבלה כך יובשה על MgSO4 וסוננה.לאחר מכן, התסנין רוכז בוואקום כדי להשיג את תרכובת האובייקט (שמן חסר צבע, כמותי); 1HNMR (200 MHz, CDCl3) דלתא 3.74 (q, J= 10.5, 5.2 Hz, 2H) 3.25 (t, J= 5.2 Hz, 2H) 2.91 (s, 3H) 1.45 (s, 9H);ספקטרום מסה m/e (עוצמה יחסית) 144 (20) 102 (24) 57 (70) 44 (100).
2-(מתילאמינו)אתנול (90.1 גרם, 1.2 מול) הומס ב-1.2 ליטר מתילן כלוריד, ו-BoC2O (218 גרם, 1 מול) הוספה אליו באיטיות תוך כדי ערבוב ב-00C, ולאחר מכן בטמפרטורת החדר למשך 3 שעות.תערובת התגובה נשטפה ברצף עם 700 מ"ל של תמיסה מימית של אמוניום כלוריד רווי ו-300 מ"ל מים.התערובת השטופה התייבשה באמצעות נתרן סולפט נטול מים ורוכזה בלחץ מופחת, לקבלת התרכובת (א) (175 גרם, 1 מול, 100%) כשמן ללא צבע. TLC : Rf = 0.5 (50% EtOAc ב Hex) הודגם עם Ce-Mo stain1H NMR (600MHz, CDCl3) דלתא 1.47 (s, 9H), 2.88 (br s, IH), 3.41 (br s, 2H), 3.76 (br s, 2H).
90.1 גרם (1.2 מול) של 2-(מתילאמינו)אתנול הומסו ב-1.2 ליטר מתילן כלוריד, 218 גרם (1 מול) של Boc2O הוספו אליו באיטיות תוך כדי בחישה של התמיסה שהתקבלה ב-0C, והתמיסה שהתקבלה נערבלה בשעה טמפרטורת החדר למשך 3 שעות.תערובת התגובה נשטפה ברצף עם 700 מ"ל של תמיסת אמוניום כלוריד רוויה מימית ו-300 מ"ל מים, התייבשה באמצעות נתרן גופרתי נטול מים, ולאחר מכן רוכזה בלחץ מופחת לקבלת 175 גרם (1 מול) של תרכובת שמן אכרומית מוגנת על ידי קבוצת בוק (תשואה: 100%).[0140] 1H NMR (600MHz, CDCl3) דלתא 7.84 (br s, 2H), 7.76 (br s, 2H), 4.34 (d, J = 15.0 Hz, 2H), 3.63 (br s, 2H), 3.04 (d , J = 15.0 הרץ, 3H), 1.46 (ד, J = 16.2 הרץ, 9H) [0141] 90 גרם (0.514 מול) מהתרכובת שהתקבלה הומסו ב-1.5 ליטר טטרהידרופורן, 88.0 גרם (539 מול) של N- נוספו אליו הידרוקסיפתלימיד ו-141 גרם (0.539 מול) טריפניל-פוספין, 106 מ"ל (0.539 מול) של דיאיזופרופיל אזודיקרבוקסילאט נוספו אליו באיטיות תוך ערבוב התמיסה שהתקבלה ב-0C, והתמיסה שהתקבלה נערכה במשך 3 שעות תוך העלאת הטמפרטורה שלה. לטמפרטורת החדר.לאחר ריכוז תערובת התגובה בלחץ מופחת, נוספו אליה 600 מ"ל של איזופרופילתר, התמיסה שהתקבלה עורבבה ב-0C למשך שעה אחת, ותחמוצת טריפנילפוספין לבנה מסוג מוצק סונן.המוצק נשטף עם 200 מ"ל של איזופרופילתר שצונן ל-0C ונאסף עם התסנין הראשון, והתסנין שהתקבל רוכז בלחץ מופחת לקבלת 198 גרם של תערובת של תרכובת XX ודיאיזופרופיל הידראזודיקארבוקסילט ביחס ערבוב של 10 עד 15% (תשואה: 120%).[0142] 1H NMR (600MHz, CDCl3) דלתא 7.84 (br s, 2H), 7.76 (br s, 2H), 4.34 (d, J = 15.0 Hz, 2H), 3.63 (br s, 2H), 3.04 (d , J = 15.0 הרץ, 3H), 1.46 (ד, J= 16.2 הרץ, 9H)
 בניין 12, מס' 309, דרום כביש 2, אזור פיתוח כלכלי, מחוז לונגקוואני, צ'נגדו, סצ'ואן, סין.
בניין 12, מס' 309, דרום כביש 2, אזור פיתוח כלכלי, מחוז לונגקוואני, צ'נגדו, סצ'ואן, סין. amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com
amy@enlaibio.com / cynthia@enlaibio.com / edison@enlaibio.com / daisy@enlaibio.com +86 (028) 84841969
+86 (028) 84841969 +86 135 5885 5404
+86 135 5885 5404



















.png)


